Idéia de material
Por Redação
3. Idéia de material
Matéria, ou material é tudo aquilo que possui massa, ocupando um lugar no espaço.
Exemplos: ar, água, terra, ferro etc.
Corpo: é um fragmento limitado de matéria.
Exemplo: um pedaço de ferro ou de madeira etc.
Toda matéria é composta por átomos. A forma, na qual estes átomos estão organizados é como podemos diferenciá-los em: elemento químico, substância pura e mistura.
Elemento químico
Há muito tempo, cerca de 30 anos antes de Cristo, o filósofo grego Demócrito já afirmava que a matéria era formada por partículas muito pequenas, às quais ele chamou de átomos e que a terra, o fogo, a água e o ar, eram elementos de extrema importância e fundamentais.
Porém, sua teoria fora recusada por Aristóteles, que era adepto de que a matéria é continua e seus argumentos sem restrições.
E no século XVII, surgiu à explicação sobre o comportamento de gases sobre a movimentação das partículas, proposição criada por Newton que superou a teoria de Aristóteles. A teoria de Newton foi adaptada na compreensão da combinação da proporção das reações de substâncias químicas, por Higgins. Nesse mesmo século Robert Boyle opõe-se à teoria dos quatro elementos formadores, porém não se opõe sobre a teoria dos átomos.
A partir do século XVIII foi concluído que existe mais de quatro elementos, descoberta feita por Lavoisier que construiu uma lista de 23 elementos. Por volta do século XIX Dalton afirma que as propriedades da matéria podem ser averiguadas e compreendidas em termos comportamentais das partículas finitas concluídas a partir da definição de massas relativas dos átomos.
Foram feitas outras experiências que concluem que o átomo é composto por partículas bem menores.
Os fundamentais aspectos da teoria de Dalton:
– os átomos são sólidos e indivisíveis;
– átomos compostos de elementos diferentes são diferentes;
– na formação dos compostos é necessário que os átomos dos elementos se relacionem ás proporções simples e fixas.
Os elementos químicos são formados por átomos idênticos entre si.

A) Símbolos
Os elementos químicos são organizados por nomes e símbolos diferentes.
Eles são apresentados pela primeira letra de seu nome (maiúscula), quando há nomes que iniciam com a mesma letra acrescentasse mais uma letra minúscula. Alguns elementos são representados pela primeira letra do “seu” nome em latim.
Veja abaixo alguns exemplos:
hidrogênio – H
Helio – He
Sódio – Na (natrium)
Fósforo – P (Phosphoro)
Cobre – Cu (Cuprum)
Mercúrio – Hg (Hidrargirium)
Chumbo – Pb ( Plumbum)
O símbolo pode significar o átomo como o elemento.

O elemento químico é formado por átomos idênticos, porém existem mais de 100 diferentes tipos de elementos químicos.
B) Princípio da idéia de molécula
Normalmente os átomos se agrupam, resultando na formação de moléculas.
Exemplo:
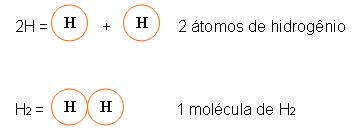
a) 2 átomos de O juntos, dão origem à molécula do gás oxigênio.
![]()
b) 2 átomos de H juntos dão origem à uma molécula do gás hidrogênio.
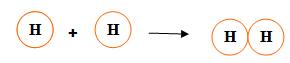
c) 2 átomos de H e 1 átomo de O juntos, dão origem à uma molécula de água.
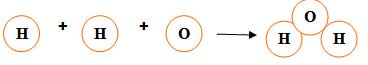
Concluímos então que as moléculas são consideradas a junção de átomos que estão interligados entre si, podendo ser iguais ou diferentes.
Substância pura
A substância nada mais é que uma matéria composta por um único e igual tipo de substância, como por exemplo, a amônia onde todas as suas moléculas são iguais e possui a fórmula NH3, e o gás nitrogênio, onde todas as moléculas são iguais e possuem fórmula N2.
A) Fórmula
É através da fórmula que conseguimos representar uma molécula de uma substância qualquer, como nos mostra a ilustração abaixo:
Exemplo:



Existem também os índices, que são os números presentes nas fórmulas. Eles apontam a quantidade de átomos presente nas moléculas, de cada um dos elementos químicos. É importante ressaltar que quando o índice for 1, ele não precisará aparecer na fórmula. Vejamos:

Porém é necessário atentar-se à algumas observações, sabendo diferenciá-las: Vejamos:
A forma certa de dizer é que na fórmula da água, ou seja, em uma molécula H2O existem dois átomos de H e um de O.
Observe como é representada graficamente três moléculas de hidrogênio.
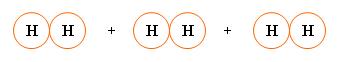
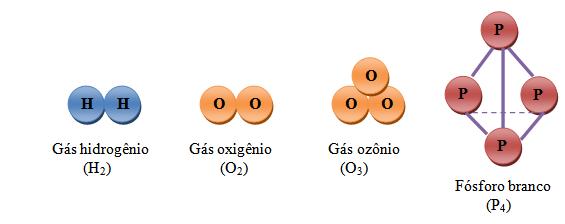
B) Substância simples
A substância simples é formada por apenas um único tipo de molécula e átomo.
Exemplos:
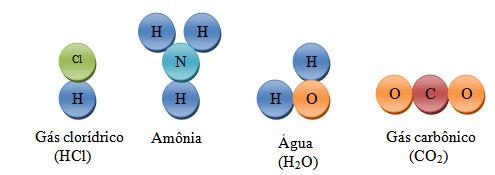
C) Substância composta
As substâncias composta ou compostos, são formadas por átomos que contém mais de um tipo de elemento químico.
Exemplo:
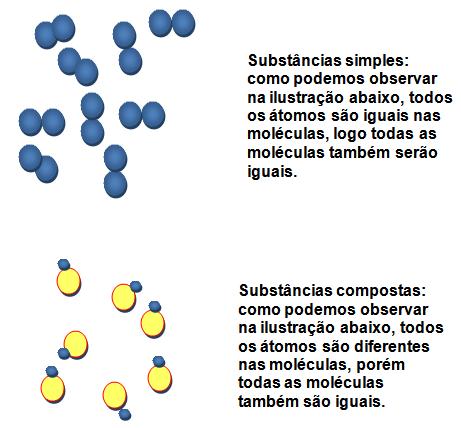
D) Divergência entre substância simples e composta
E) Conceituação de molécula
É a partícula de menor tamanho que pode existir em uma substância pura contendo ainda nessa partícula as propriedades químicas da substância original que foi dividida inúmeras vezes.
Concluímos então que uma substância pura e composta por uma espécie de molécula específica e substâncias diferentes é composta diferentemente.
Vejamos um exemplo:
Se misturarmos uma colher de açúcar em um copo de água, o açúcar se dissolve na água fazendo com que não seja possível mais visualizar as moléculas.
Mistura
É qualquer sistema formado por duas ou mais substâncias puras. Não apresentam “constantes físicas” definidas; ponto de fusão, ebulição, densidade absoluta, mudam com a composição da mistura.
As misturas não apresentam uma representação específica, mas é comum ver algumas misturas representadas por seus componentes. Entretanto, existem misturas que possuem nomes específicos, por exemplo:
Álcool 96% G.L(grau Gay Lussac, que indicador da porcentagem de álcool) de álcool, 4% de água.
Ouro 18K (quilates) mistura de 75% de ouro e 25% de cobre.
Bronze é a mistura de cobre e estanho.

 Separação de misturas
Separação de misturas