BERZELIUS
“Somente os seres vivos podem transformar substâncias minerais em orgânicas.” (Teoria da Força Vital)
WHÖLLER
Síntese da ureia (composto orgânico) a partir do cianato de amônio” (composto inorgânico) em laboratório.
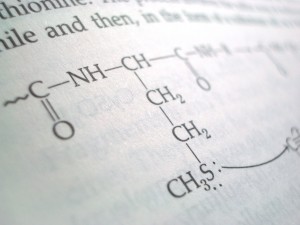
NH2
NH4CNO C = O
/
NH2
Características do carbono
Postulados de Kekulé:
a) É tetracovalente.
b) Os ângulos entre as valências são de 109º 28’, adquirindo a forma de um tetraedro regular.
c) Possui a propriedade de encadeamento.
d) Um átomo de carbono pode formar uma, duas ou até três ligações com um segundo átomo, realizando, assim, respectivamente, ligações simples, duplas ou triplas.
Assim, classificamos as ligações do carbono em:
a) Sigma ( 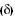
b) Pi ( 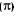
Número de átomos de C unidos diretamente a ele:
• Carbono primário.
• Carbono secundário.
• Carbono terciário.
• Carbono quaternário.
Saturação
SATURADO: é aquele que apresenta apenas simples ligações;
C — C — C — C
INSATURADO: aquele que apresenta dupla ou tripla ligação:
C = C – C – C ou C º C
Hibridização do Carbono
1. sp3 (tetraédrica)
a) é a fusão de quatro orbitais (um do tipo s e três do tipo p) formando quatro orbitais do tipo sp3;
b) forma somente ligações simples;
c) ângulo entre as valências: 109º 28’;
d) é característica dos alcanos;
e) carbono liga-se a outros quatro átomos.
2. sp2 (trigonal)
a) é a fusão de um orbital s com dois orbitais p, formando três orbitais do tipo sp2;
b) forma duas ligações simples e uma dupla;
c) ângulo entre as valências: 120º;
d) é característica dos alcenos;
e) carbono liga-se a outros três átomos.
3. sp (linear)
a) é a fusão de um orbital s com um p formando dois orbitais do tipo sp;
b) pode formar duas ligações duplas ou uma tripla e uma simples;
c) ângulo entre as valências: 180º;
d) é característica dos alcinos e alcadienos;
e) carbono liga-se a outros dois átomos.