4. Conceito de oxidação e redução
Oxidação
Se tratando de oxidação, podemos dizer que ela é considerada a transformação onde ocorre um aumento do número de oxidação das espécies químicas.
A oxidação é relacionada com um fenômeno químico (combinar com o oxigênio), portanto toda espécie que combinar com o oxigênio, irá sofrer uma oxidação. Já se um átomo se combinar com o oxigênio, ele terá a tendência de perder elétrons, aumentando assim o número de oxidação no carbono.
Vamos imaginar que um prego de ferro, sofreu uma oxidação, ou seja, ele perdeu elétrons, logo se colocarmos em forma de equação, veremos que o seu número de oxidação aumentou.
Vejamos:
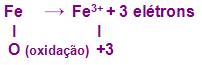
Portanto a partir das afirmações acima, podemos dizer que o fenômeno oxidação “significa” a perda de elétrons.
Redução
Se tratando de redução, podemos dizer que ela é considerada uma transformação onde ocorre uma diminuição do número de oxidação de uma espécie química.
Observe abaixo a reação entre magnésio e oxigênio, no formato eletrônico.
Mg (Z = 12)
O (Z = 8)
|
K |
L |
M |
|
2 |
8 |
2 |
|
2 |
6 |
Obs.: o flúor é o único elemento cujo os átomos não perdem elétrons ao se combinarem, ao contrário de todos os átomos.
Vejamos agora uma figura que nos mostra que o magnésio sofreu uma oxidação, perdendo assim dois elétrons, consequentemente o oxigênio sofreu uma redução, ganhando assim dois elétrons. Vejamos a ilustração abaixo:
Observando a figura nota-se que o magnésio perdeu 2 elétrons, ocorrendo a oxidação, neste caso o oxigênio recebeu 2 elétrons, decorrente da redução que sofreu.
