Subníveis de energia
Por Redação
Os níveis de energia são subdivididos em subníveis de energia, quando a energia é liberada, podemos dizer que ocorreu uma radiação. O número quântico de um elétron varia de acordo com o subnível e cada um tem uma quantidade máxima:

Notação da configuração eletrônica
Observe o a tabela:
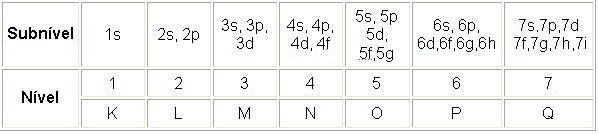
Os subníveis estão representados na ordem energética.
Exemplo:
3p5 : Onde 3 é número quântico principal, p é letra que indica o subnível e 5 é a quantidade de elétrons.
Métodos que servem para o ordenação dos subníveis
1) Método analítico
n + l é a proporção da soma de um subnível, n representa o número quântico principal, e l representa os números secundários.
Observe os exemplos e veja que 4s é menos energético que 3d.

É importante lembrarmos que o subnível que terá maior energia irá ser o que ficar mais afastado, dentre aqueles que apresentarem a mesma soma.
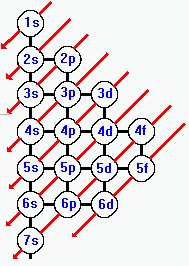
2) Método gráfico
Podemos obsevar claramente no Diagrama de Linus Pauling conforme as linhas diagonais descem, a energia sobe. Vejamos: