Tipos de constante de equílibrio
Por Redação
8. Tipos de constante de equilíbrio
Podemos expressar a constante de equilíbrio de duas maneiras:
Kc: constante de equilíbrio expressa em função de quantidade de matéria (mol/L).
Kp: constante de equilíbrio expressa em função das expressões parciais.
Apresentamos a constante Kc colocando na fórmula os valores das concentrações, em mol/L, no equilíbrio.
Apresentamos a constante Kp colocando na fórmula os valores das pressões parciais dos gases presentes no equilíbrio (em atm ou mmHg).
Exemplos de aplicação das constantes
1)

2)

3)

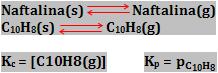
Na expressão Kc não participam substâncias sólidas, somente concentrações que podem sofrer variações, como a concentração de uma substância em solução e a concentração de um gás.
![]()
Na expressão Kp somente participam substâncias gasosas.
4)

5)

6)
Todas as reações químicas possuem um determinado valor para cada constante de equilíbrio. Tal valor depende da temperatura.
Portanto, podemos dizer que, a constante de equilíbrio depende da reação química e da temperatura.
Logo,
Só ocorrerá alterações nas constantes Kc e Kp, quando ocorrer variações na temperatura.
