2. A célula eletrolítica
A célula é um dispositivo formado por dois eletrodos: A (ânodo) e C (cátions), submergidos num líquido contido de íons livres, como o M+ e X–.

Seja o composto genérico MX. Numa solução aquosa, ele dissocia:
MX → M+ + X–
Veja o que ocorre utilizando a energia elétrica:
Redução no cátodo
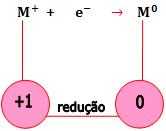
Redução do ânodo
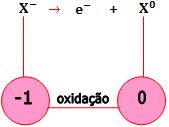
Os ânions cedem elétrons para o ânodo. Os elétrons percorrem o circuito. Os cátions recebem elétrons do cátodo.
Liga-se uma bateria aos eletrodos A e C através de dois fios. A bateria bombeia elétrons, empurrando-os para o eletrodo C e retirando-os do eletrodo A.
Ao fornecer energia elétrica para uma célula eletrolítica, ocorre a eletrólise. Conclusão: a célula eletrolítica transforma a energia elétrica em energia química.
A liberdade de movimento dos íons pode ser adquirida através da:
– fusão: eletrólise ígnea
– dissolução em um solvente polar: eletrólise em solução.