10. Semi-reação de oxidação e redução
Seja uma reação que ocorre quando submergimos uma barra de zinco numa solução contida de íons Cu+2, obtida através da dissolução de sulfato de cobre em água.
Normalmente, a reação que ocorrerá pode ser representada pela equação abaixo:
Zn(s) + CuSO4(aq) → ZnSO4(aq) + Cu(s)
Os sais estão dissociados:
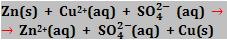
Veja que os íons não participam de fato da reação:
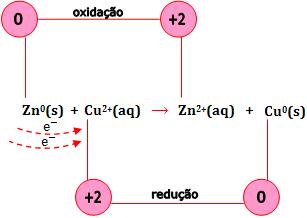
A reação é formada a partir de uma conversão de elétrons do átomo de zinco para o íon Cu2+.
Na reação citada, cobre metálico é depositado na superfície do zinco e a cor azul do íon Cu2+ oculta-se quando é substituído pelo íons Zn+2 incolor.
A reação pode ser dividida em duas partes:

Ao somar as duas semi-reações, obtemos a reação global. Veja que o número de elétrons cedidos é igual ao número de elétrons recebidos.