Reação de neutralização segundo a teoria de Arrhenius
Por Redação
11. Reações de neutralização segundo a teoria de Arrhenius
É preciso considerar algumas informações sobre a reação de um ácido com uma base. Vejamos:
• Os ácidos covalentes que estão ionizados, conseqüentemente estão em solução aquosa, logo em uma reação de neutralização o HCl, irá aparecer da seguinte maneira: vejamos:
H+ Cl–
• As bases em solução aquosa ficam dissociadas, e são consideradas compostos iônicos, logo em uma reação o NaOH irá aparecer da seguinte maneira:
Na+ e OH–
• Os sais, compostos iônicos na presença de soluções aquosas fica dissociado, logo em uma reação o NaCl irá aparecer da seguinte maneira:
Na+ e Cl–
Observe abaixo a equação da reação de HCl e NaOH, considerando as informações anteriores:
H+ (aq) + Cl–(aq) + Na+ (aq) + OH–(aq) → Na+ (aq) + Cl–(aq) + H2O(l)
De forma mais simplificada:
![]()
Vejamos agora outro exemplo com outra reação:
H2SO4 + KOH → KHSO4 + H2O
H+ + HSO-4 + K+ + OH– → K+ + HSO-4 + H2O
H+ + OH– → H2O
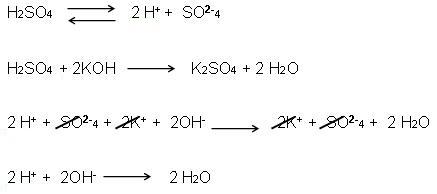
Agora observe a mesma reação, com a equação global, ou seja, a soma do H2SO4: