Fórmulas estruturais e eletrônicas dos ácidos
Por Redação
5- Fórmulas estruturais e eletrônicas dos ácidos
– hidrácidos
Observe abaixo fórmula eletrônica de alguns dos hidrácidos:
Ácido fluorídrico: H – F Acido iodídrico: H – I Ácido clorídrico: H – Cl
– Ácidos orgânicos
Os ácidos orgânicos são ácidos carboxílicos, pelo fato de conterem a presença de carboxilas, que possuem hidrogênios que podem ser ionizados.
Carboxila
![]() Os ácidos: ácidos fórmicos, ácidos acético, ácido oxálico, apresentam hidrogênios ionizável.
Os ácidos: ácidos fórmicos, ácidos acético, ácido oxálico, apresentam hidrogênios ionizável.
– Para escrever a fórmula estrutural de um oxoácido é necessário respeitar algumas regras, vejamos:
Regra número 1
É preciso escrever o símbolo do átomo central, por exemplo: Cl.
Regra número 2
É necessário ligar o átomo central aos grupos OH que forem ionizáveis (hidrogênios).
Regra número 3
É necessário ligar o átomo central aos hidrogênios não-ionizáveis se caso tiver hidrogênio não ionizável.
Regra número 4
Para que o octeto fique completo, é necessário que o átomo central esteja ligado aos átomos de oxigênio que sobrou, essa ligação deve ser por dupla ou dativa, de acordo com o que for necessário.
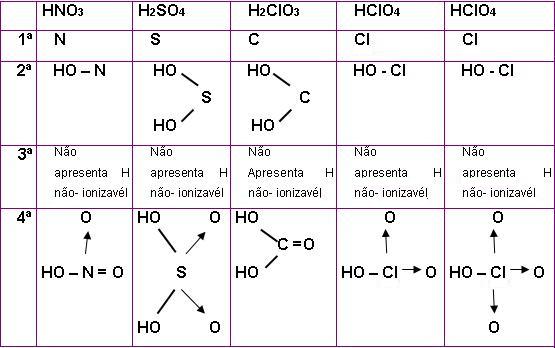
Para transformar as fórmulas estruturais em fórmula eletrônica é necessário apenas, trocar as ligações covalentes e dativas por pares de elétrons.
Particularidades
– Peroxiácidos
Peroxiácidos são todos os ácidos que em sua molécula contêm um grupo peróxi, ou seja, – O – O –.
Por exemplo:
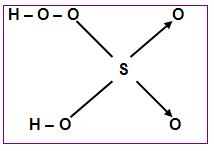
Ácido peroximonossulfúrico (H2SO5)
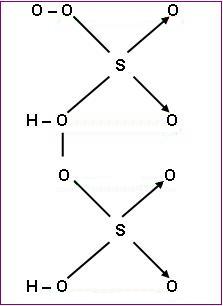
Ácido peroxidissulfúrico (H2S2O5)
– Tioácidos
É capaz de substituir um átomo de oxigênio por um átomo de enxofre.
Por exemplo:
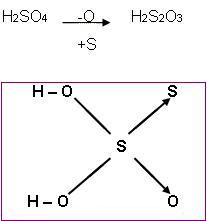
Ácido tiossulfúrico
