6- Variação das propriedades de acordo com a posição na tabela periódica
Tamanho dos átomos
Carga nuclear
É o número de prótons, ele dispõe-se a aproximar os elétrons para perto do núcleo.
Efeito de Proteção dos elétrons Internos
É para evitar que os elétrons externos cheguem muito perto do núcleo.
Existe um problema, que é o de identificar qual dos fatores que atuam é mais forte, e produzem efeitos opostos.
Observe na ilustração abaixo que o átomo é maior que o seu cátion, e o ânion é maior que o átomo respectivo.
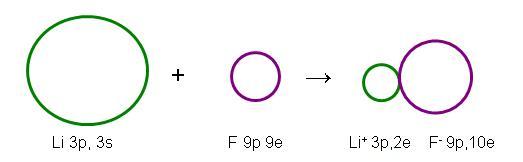
Variação do tamanho atômico dentro dos grupos:
Conforme ocorre aumento de número atômico, os átomos aumentam o tamanho, dentro do grupo, devido ao efeito dos níveis intermediários que aumenta o raio, predominando sobre o efeito de maior carga nuclear, resultando na diminuição do raio. Observe abaixo:
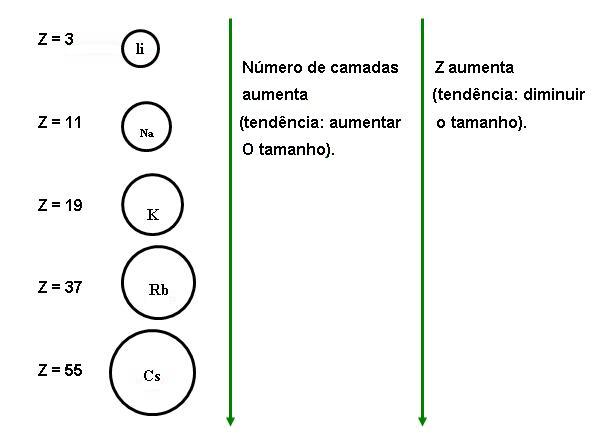
Variação do tamanho atômico dentro dos períodos:
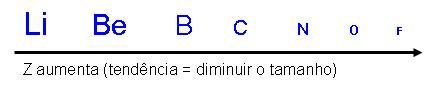
Observe que cada período de Li para f, os átomos diminuem de tamanho, pelo fato de ocorrer o aumento da carga no núcleo, e o número quântico principal não sofre alterações, portanto ele continua constante.
Raios atômicos, covalente, iônico e de Van de Waals:
Para medir a distância entre dois núcleos de dois átomos, utilizam-se medidas com raios-X em cristais, pois é difícil descobrir onde acaba um átomo pela pouca nitidez das nuvens de elétrons.
A distância d depende da ligação dos átomos, desta forma existem 4 tipos de raio, são os raio atômico, raio iônico, raio covalente, raio de Van Der Waals ou raios de colisão.
Vejamos cada um deles:
– Raio atômico
O raio atômico é considerado a metade da distância existente entre o centro de um átomo e o núcleo. Observe os exemplos dos raios atômicos dos metais alcalinos:
Li – 1,52 Å
Na – 1,86 Å
K – 2,31 Å
Rb – 2,44 Å
Cs – 2,62 Å
Fr – 2,7 Å
– Raio iônico
Quando falamos a respeito do cristal iônico, dizemos que a distância existente entre os íons de carga contrária é a soma dos raios iônicos tanto dos cátions como dos ânions.
Vejamos agora uma ilustração que nos mostra que certa distância representada po Y, é considerada a soma dos cátions e dos ânions, portanto podemos dizer que a distância X é considerada o dobro do raio do ânion.
– Raio covalente
Com relação a distância entre alguns átomos ligados através de uma ligação covalente, dizemos que ela é a união de dois raios covalentes. Caso os átomos sejam idênticos o raio será a metade da distância entre núcleos, ou seja:
– Raio de Van der Waals ou raio de colisão
Johannes Diederik Van Der Waals, físico neerlandês.
É chamado raio de Van Der Waals ou raio de colisão, somente a metade da distância internuclear, porém quando os átomos não estão ligados através de ligações.